Bilangan kuantum (bahasa inggris: Quantum number) adalah bilangan yang menyatakan kedudukan atau posisi elektron dalam atom yang diwakili oleh suatu nilai yang menjelaskan kuantitas kekal dalam sistem dinamis. Bilangan kuantum menggambarkan sifat elektron dalam orbital. Bilangan kuantum menentukan tingkat energi utama atau jarak dari inti, bentuk orbital, orientasi orbital, dan spin elektron. Setiap sistem kuantum dapat memiliki satu atau lebih bilangan kuantum.
Bilangan kuantum merupakan salah satu ciri khas dari model atom mekanika kuantum atau model atom modern yang dicetuskan oleh Erwin Schrodinger. Dalam mekanika kuantum, bilangan kuantum diperlukan untuk menggambarkan distribusi elektron dalam atom hidrogen dan atom-atom lain. Bilangan-bilangan ini diturunkan dari penyelesaian matematis persamaan schordinger untuk atom hidrogen.: (wikipedia)
Macam- Macam Bilangan Kuantum :
1. Utama (n)
Bilangan
kuantum utama (lambang n) sesuai dengan bilangan n yang
digunakan oleh Bohr untuk menentukan energi total elektron. Energi total
elektron bertanda negatif, yang berarti bahwa untuk mengeluarkan elektron
sehingga bebas dari grbitnya diperlukan energi. Energi total elektron
terkuantisasi artinya hanya dapat memiliki harga tertentu/diskret. Perhatikan,
energi total elektron hanya bergantung pada n dan tidak pada bilangan-bilangan
kuantum lainnya. Untuk atom hidrogen, energi total elektron dinyatakan oleh:(pelajaran, 2016)
2. Azimut ( l )
Bilangan kuantum azimut adalah bilangan yang menggambarkan
subkulit atau subtingkat energi utama yang dinotasikan dengan l. Bilangan
kuantum azimut menentukan bentuk orbital dari elektron.
Notasi huruf digunakan untuk menunjukkan berbagai nilai l.
Bentuk orbital dengan bilangan kuantum azimut sama dinamakan subkulit. Jadi, bilangan kuantum azimut dapat juga menunjukkan jumlah subkulit dalam setiap kulit. Masing-masing subkulit diberi lambang dengan s, p, d, f, …, dan seterusnya. Hubungan subkulit dengan lambangnya adalah sebagai berikut.(pelajaran, 2016)
3. Magnetik (m)
Bilangan kuantum magnetik adalah bilangan yang menyatakan orientasi orbital dalam subkulit yang dinotasikan dengan m. Dengan demikian, setiap orbital dalam subkulit tertentu dapat dibedakan orientasi orbitalnya dengan bilangan magnetik. (onlline,
2013)
Hubungan Bilangan Kuantum Azimut dengan Bilangan Kuantum Magnetik
4. Spin ( s)
Bilangan kuantum spin menggambarkan arah rotasi atau putaran elektron dalam satu orbital yang dinotasikan dengan s. Karena hanya ada 2 arah putaran yang mungkin yaitu searah jarum jam (clockwise) dan berlawanan arah jarum jam (anticlockwise), maka setiap orbital memuat 2 elektron dengan arah rotasi yang berlawanan. Oleh karena itu diberi nilai ± ½.
Arah rotasi pertama ditunjukkan ke atas dengan notasi s = +½ atau rotasi searah dengan arah putaran jarum jam dengan simbol ↑. Sedangkan arah ke bawah menunjukkan notasi s = -½ atau berlawanan dengan arah putaran jarum jam dengan simbol ↓.(nafiun, Pengertian Bilangan Kuantum Utama, Azimut,
Magnetik, Spin, Contoh Soal, Kunci Jawaban, 2013)
Konfigurasi elektron
Konfigurasi elektron dalah konfigurasi yang menggambarkan susunan elektron dalam orbital-orbital atom. Dengan mengetahui konfigurasi elektron, jumlah elektron pada kulit terluar dapat ditentukan.(nafiun,
Prinsip Aufbau, Aturan Hund dan Larangan Pauli, Asas, Kaidah, Konfigurasi
Elektron, Kimia, 2013)
1. Asas Aufbau
pengisian elektron dimulai dari tingkat energi terendah menuju tingkat energi yang lebih tinggi. Prinsip ini dikenal dengan prinsip Aufbau. Keadaan ketika elektron mengisi kulit dengan energi terendah disebut keadaan dasar (ground state).(nafiun,
Prinsip Aufbau, Aturan Hund dan Larangan Pauli, Asas, Kaidah, Konfigurasi
Elektron, Kimia, 2013)
Urutan tingkat energi pada orbital
Arah anak panah menyatakan urutan pengisian orbital. [1] Urutan orbital berdasarkan tingkat energi mengacu pada urutan arah panah, yaitu 1s, 2s, 2p, 3s, 3p, dan seterusnya. Dari urutan tersebut terlihat bahwa tingkat energi 3d lebih besar dibandingkan tingkat energi 4s. Jadi, setelah 3p penuh, elektron akan mengisi subkulit 4s terlebih dahulu sebelum subkulit 3d.(nafiun,
Prinsip Aufbau, Aturan Hund dan Larangan Pauli, Asas, Kaidah, Konfigurasi
Elektron, Kimia, 2013)
Contoh 1
Tentukan konfigurasi elektron unsur-unsur berikut berdasarkan prinsip Aufbau.
a. 15P
b. 26Fe
Jawaban :
a. 15P : 1s1 2s2 2p6 3s2 3p3
b. 26Fe : 1s1 2s2 2p6 3s2 3p6 4s2 3p6
2, Aturan Hund
Frederick Hund, 1927 (dikenal Hund) menyatakan bahwa elektron yang mengisi subkulit dengan jumlah orbital lebih dari satu akan tersebar pada orbital yang mempunyai kesamaan energi (equal-energy orbital) dengan arah putaran (spin) yang sama. (nafiun,
Prinsip Aufbau, Aturan Hund dan Larangan Pauli, Asas, Kaidah, Konfigurasi
Elektron, Kimia, 2013)
Contoh pengisian yang benar.

Subkulit yang mengandung orbital lebih dari 1 adalah p, d, dan f. Pengisian elektron menurut aturan hund dimulai dengan mengisi satu elektron pada tiap-tiap orbital dengan arah putaran (spin) yang sama. Setelah semua orbital terisi satu elektron, elektron sisanya akan mengisi orbital dengan arah putaran (spin) yang berlawanan, sehingga orbital terisi pasangan elektron. (nafiun,
Prinsip Aufbau, Aturan Hund dan Larangan Pauli, Asas, Kaidah, Konfigurasi
Elektron, Kimia, 2013)
Contoh:
Tentukan diagram orbital untuk unsur-unsur berikut.
1. 7N
2. 9F
Jawaban :
2. 9F = 1s2 2s2 2p5
3. Asas
Larangan Pauli
Pauli mengemukakan hipotesisnya yang menyatakan bahwa dalam satu atom tidak mungkin dua elektron mempunyai keempat bilangan kuantum sama. Misal, 2 elektron akan menempati subkulit 1s. Tiga bilangan kuantum pertama akan mempunyai nilai yang sama (n = 1, l = 0, m = 0). Untuk itu bilangan kuantum yang terakhir, yaitu bilangan kuantum spin(s) harus mempunyai nilai berbeda (+1/2 atau -1/2).
Dengan kata lain, setiap orbital maksimal hanya dapat terisi 2 elektron dengan arah spin berlawanan. Sebagai contoh, pengisian elektron pada orbital 1s digambarkan sebagai berikut. (nafiun,
Prinsip Aufbau, Aturan Hund dan Larangan Pauli, Asas, Kaidah, Konfigurasi
Elektron, Kimia, 2013)
Jumlah elektron maksimal untuk tiap subkulit sama dengan dua kali dari jumlah orbitalnya.
(nafiun, Prinsip Aufbau, Aturan Hund dan Larangan Pauli, Asas, Kaidah, Konfigurasi Elektron, Kimia, 2013)
(nafiun, Prinsip Aufbau, Aturan Hund dan Larangan Pauli, Asas, Kaidah, Konfigurasi Elektron, Kimia, 2013)
- orbital s maksimal 2 elektron
- orbital p maksimal 6 elektron
- orbital d maksimal 10 elektron, dan
- orbital f maksimal 14 elektron.
Contoh :
Tentukan bilangan kuantum dan diagram orbital yang dimiliki oleh atom-atom berikut.
a. 20Ca
Jawaban :
a. 20Ca= (Ar) 4s2
n = 4, l = 0, m = 0, dan s = - ½
Daftar pustaka
masuk, g. (2015, 10). Konfigurasi Elektron ( Asas
Aufbau, Larangan Pauli dan Hund). Diambil kembali dari
https://sainsmini.blogspot.com/2015/10/konfigurasi-elektron-asas-aufbau.html
nafiun. (2013, 04). Pengertian Bilangan Kuantum
Utama, Azimut, Magnetik, Spin, Contoh Soal, Kunci Jawaban. Diambil
kembali dari http://www.nafiun.com/2013/04/pengertian-bilangan-kuantum-utama-azimut-magnetik-spin-contoh-soal-kunci-jawaban.html
nafiun. (2013, 07). Prinsip Aufbau, Aturan Hund
dan Larangan Pauli, Asas, Kaidah, Konfigurasi Elektron, Kimia. Diambil
kembali dari http://www.nafiun.com/2013/04/prinsip-aufbau-aturan-hund-dan-larangan-pauli-asas-kaidah-konfigurasi-elektron-kimia.html
onlline, b. k. (2013). PENGERTIAN BILANGAN
KUANTUM. Diambil kembali dari
https://belajarkimiaonlineyuk.wordpress.com/bilangan-kuantum/materi/pengertian-bilangan-kuantum/
pelajaran. (2016, 08). Atom Berelektron Banyak –
Bilangan Kuantum Utama, Orbital, Magnetik dan Kuantum Spin. Diambil
kembali dari
https://www.pelajaran.co.id/2016/08/atom-berelektron-banyak-bilangan-kuantum-utama-orbital-magnetik-dan-kuantum-spin.html
Sma, M. K. (2013, 07). Bilangan Kuantum Azimut (
l ). Diambil kembali dari
https://materi-kimia-sma.blogspot.com/2013/07/bilangan-kuantum-azimut.html
wikipedia. (t.thn.). Bilangan kuantum.
Diambil kembali dari https://id.wikipedia.org/wiki/Bilangan_kuantum
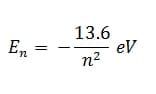











Sangat Bermanfaat
BalasHapusGood luck,, luar biasa
BalasHapusGood🐣🐣
BalasHapusMantapp
BalasHapus👍👍👍
BalasHapusmantul
BalasHapussangat membantu👍👍👍👍👍
Ntaps
BalasHapus👍👍👍
BalasHapusBagus banget
BalasHapusMantepp
BalasHapusGood job❤
BalasHapusSangat membantu✨
BalasHapussip
BalasHapusBagus, sangat membantu
BalasHapus#DISURUHYENNI
Da best kak..
BalasHapusSangat bermanfaat��
BalasHapusBagus
BalasHapusSangat bermanfaat, Good job
BalasHapusSangat bermanfaat .
BalasHapusSangat bermanfaat
BalasHapusTerima kasih, blognya sangat bermanfaat👍👍👍
BalasHapusBaguss 👍👍
BalasHapusBaguss
BalasHapusTrima kasih
BalasHapusTrima kasih
BalasHapusGood
BalasHapusMakasih nder, blog nya sangat menbantu
BalasHapusSangat bermanfaat
BalasHapusSangat membantu
BalasHapusmantapp
BalasHapusGood👌
BalasHapusmakasih informasinyaaa
BalasHapusbagus banget sangat bermanfaat, fisika saga yang tadinya 50 karna blog ini fisika saha jadi 90
BalasHapusMantul³
BalasHapusSmoga brmanfaat..
BalasHapusGood 👍👍
BalasHapusGood 👍👍
BalasHapusBermanfaat sekali, good
BalasHapusGood,semoga dapat terus membantu
BalasHapus